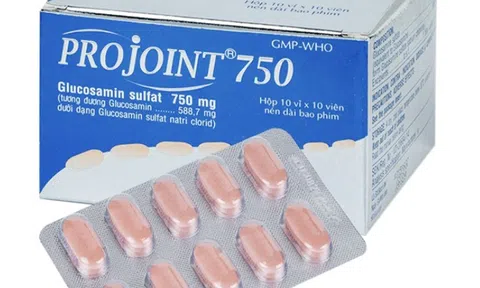
Cụ thể, lô thuốc Projoint 750 (Glucosamin sulfat 750mg) do Công ty Cổ phần Dược phẩm Cửu Long sản xuất, được phân phối bởi Công ty TNHH Thương mại Dược phẩm Việt Thành.
Sản phẩm mang SĐK: VD-20684-14, số lô: 01210524, ngày sản xuất: 21/05/2024, hạn dùng: 21/05/2027, đã được Viện Kiểm nghiệm thuốc Trung ương lấy mẫu kiểm tra tại Công ty TNHH Thương mại Dược phẩm Việt Thành.
Kết quả cho thấy thuốc không đạt tiêu chuẩn chất lượng ở chỉ tiêu "Độ hòa tan" theo tiêu chuẩn cơ sở (mức độ 3, phụ lục II Thông tư 30/2025/TT-BYT ngày 01/7/2025).
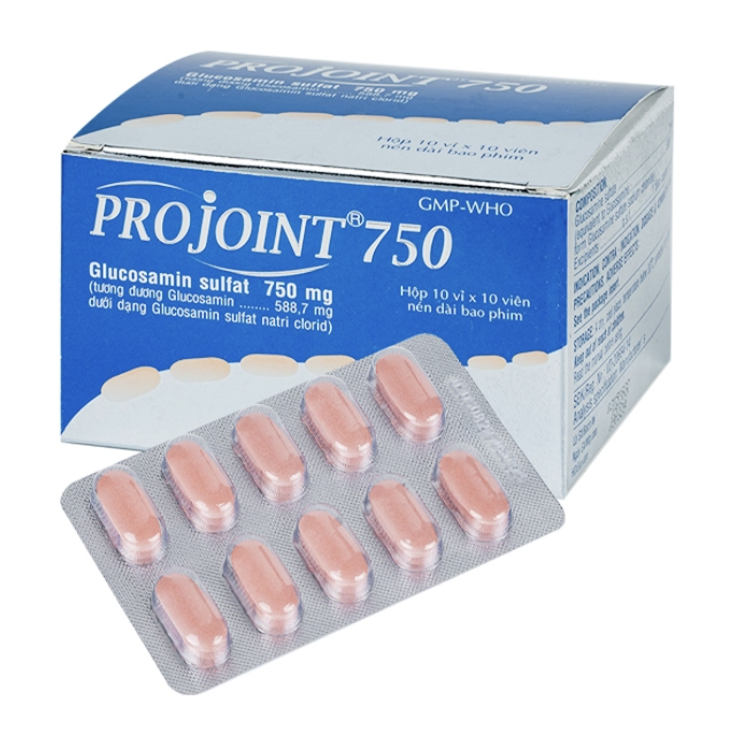
Thuốc Projoint 750 (Glucosamin sulfat 750mg) bị thu hồi vì không đạt tiêu chuẩn.
Sở Y tế Hà Nội yêu cầu Công ty Việt Thành phối hợp với Công ty Dược phẩm Cửu Long trong vòng 2 ngày kể từ khi nhận công văn phải thông báo và thu hồi toàn bộ lô thuốc vi phạm tại các cơ sở kinh doanh dược, cơ sở khám chữa bệnh trên địa bàn Hà Nội cũng như các địa phương khác có liên quan.
Đồng thời, các đơn vị này phải báo cáo kết quả thu hồi Cục Quản lý Dược, Sở Y tế Hà Nội trong thời hạn 18 ngày kể từ ngày ký công văn này, bao gồm về số lượng nhập, số lượng phân phối, số lượng thu hồi trên địa bàn Hà Nội, các bằng chứng về việc thực hiện thu hồi tại cơ sở bán buôn, bán lẻ, sử dụng đã mua thuốc theo quy định hiện hành.
Phối hợp với cơ quan kiểm tra chất lượng, cơ quan kiểm nghiệm thuốc Nhà nước tiến hành lấy mẫu bổ sung tại ít nhất 02 cơ sở kinh doanh sử dụng thuốc theo quy định tại Khoản 4 Điều 14 Thông tư 30/2025/TT-BYT ngày 01/7/2025).
Gửi mẫu đã lấy tới Viện kiểm nghiệm thuốc Trung ương để kiểm tra chất lượng đối với chỉ tiêu Độ hoà tan. Báo cáo việc thực hiện trong vòng 15 ngày kể từ ngày ký công văn này. Báo cáo kết quả kiểm tra chất lượng về Cục Quản lý Dược để có căn cứ xử lý tiếp theo.
Sở Y tế Hà Nội cũng đề nghị tất cả cơ sở y tế, nhà thuốc, quầy thuốc trên địa bàn khẩn trương rà soát, ngừng bán và thu hồi ngay lô thuốc không đạt tiêu chuẩn. UBND các xã, phường có trách nhiệm thông báo rộng rãi đến các cơ sở hành nghề y dược, đồng thời kiểm tra, giám sát chặt chẽ việc thực hiện thu hồi.